Ион арения - Arenium ion - Wikipedia

An арений ион в органическая химия циклогексадиенил катион который появляется как реактивный промежуточный продукт в электрофильное ароматическое замещение.[1] По историческим причинам этот комплекс также называют Веланд промежуточныйв честь американского химика Джорджа Уилларда Уиланда (1907–1976),[2][3] или сигма комплекс или же σ-комплекс. Наименьший ион арения - это бензиновый ион (C
6ЧАС+
7), который протонирован бензол.
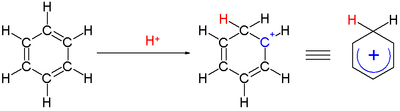
Два атома водорода, связанные с одним углеродом, лежат в плоскости, перпендикулярной бензольному кольцу.[4] Ион арения больше не является ароматическим веществом; однако он относительно стабилен из-за делокализации: положительный заряд делокализован на 3 атома углерода система пи, как показано на следующем резонансные структуры:
Комплексный электрофил может способствовать стабильности ионов арения.
Ион бензола можно выделить как стабильное соединение, когда бензол протонируется карборана суперкислота H (CB11H (CH3)5Br6).[5] Бензолевая соль кристаллическая с термической стабильностью до 150 ° C. Длина скрепления выведено из Рентгеновская кристаллография согласуются со структурой циклогексадиенильного катиона.
В одном исследовании ион метилен арения стабилизируется комплексообразованием металла:[6]
В этой последовательности реакций исходный комплекс R – Pd (II) –Br 1 стабилизируется TMEDA конвертируется через dppe к металлический комплекс 2. Электрофильный атака метилтрифлат образует метилен арений ион 3 с (на основе Рентгеновская кристаллография ) положительный заряд, расположенный в ароматическое пара-положение и с метиленовая группа 6 ° вне плоскости кольца. Реакция сначала с водой, а затем с триэтиламин гидролизует эфир группа.
Смотрите также
- Арил радикал
- Циклопентадиенил анион
- Комплекс Мейзенхаймера, аналогичный интермедиат в нуклеофильном ароматическом замещении
- Катион тропилия
Рекомендации
- ^ Олах, Г.А. (1972). «Стабильные карбокатионы. CXVIII. Общая концепция и структура карбокатионов, основанная на дифференциации трехвалентных (классических) ионов карбения от трехцентров связанных пяти- или четырехкоординированных (неклассических) ионов карбония. Роль карбокатионов в электрофильных реакциях». Варенье. Chem. Soc. 94 (3): 808–820. Дои:10.1021 / ja00758a020.
- ^ Смит, Майкл Б. (18 октября 2010 г.). Органическая химия: кислотно-щелочной подход. CRC Press. ISBN 9781439894620 - через Google Книги.
- ^ Веланд, Г. У. (1942). «Квантово-механическое исследование ориентации заместителей в ароматических молекулах». Варенье. Chem. Soc. 64 (4): 900–908. Дои:10.1021 / ja01256a047.
- ^ Сайкс, Питер. Руководство по механизму в органической химии. п. 130–133.[ISBN отсутствует ]
- ^ Reed, C.A .; Kim, K .; Стоянов, Э. С .; Стасько, Д .; Tham, F. S .; Мюллер, Л. Дж .; Бойд, П. Д. У. (2003). «Выделение бензин-ионных солей». Варенье. Chem. Soc. 125 (7): 1796–1804. Дои:10.1021 / ja027336o. PMID 12580605.
- ^ Поверенов, Э .; Leitus, G .; Мильштейн, Д. (2006). «Синтез и реакционная способность метиленарениевой формы катиона бензила, стабилизированной комплексообразованием». Варенье. Chem. Soc. (Коммуникация). 128 (51): 16450–1. Дои:10.1021 / ja067298z. PMID 17177364.